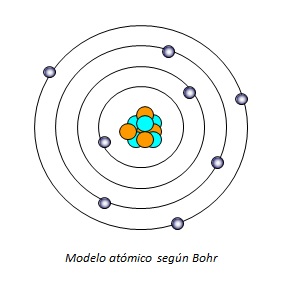
Modelo de Bohr
Niels Bohr (1885-1962)
El modelo de Bohr fue el primero en el que se aplicó la hipótesis cuántica a la estructura atómica, pretendiendo al mismo tiempo explicar los espectros discontinuos de la luz emitida por los elementos gaseosos.
Este modelo implicaba los siguientes postulados:
Niels Bohr (1885-1962)
El modelo de Bohr fue el primero en el que se aplicó la hipótesis cuántica a la estructura atómica, pretendiendo al mismo tiempo explicar los espectros discontinuos de la luz emitida por los elementos gaseosos.
Este modelo implicaba los siguientes postulados:
- Los electrones de un átomo tienen ciertos
estados definidos estacionarios de movimiento (niveles de energía) que les son
propios a cada uno; cada nivel de energía tiene un valor fijo y definido,
siendo los menos energéticos los niveles internos.
- Cuando un electrón esta en uno de estos
niveles no irradia pero cuando cambia de nivel absorbe o desprende energía y
cambia además su energía potencial en cantidades definidas.
- Cuando un electrón absorve energía pasa a un
nivel más externo, pero si un electrón pasa de un nivel externo a uno más
interno entonces se libera energía.
- La energía liberada tiene frecuencias
específicas y se muestra como un espectro de líneas y no en forma continua.
- En cualquiera de estos estados, el electrón
se mueve siguiendo una órbita circular alrededor del núcleo.
- Los valores energéticos de las orbitas de los
electrones aumentan conforme se alejan del núcleo y se representan con la letra
n. Se cuentan siete niveles de energía
1-7(representados también con letras: K, L, M, N, O, P Y Q).
- Los átomos en su estado básico tienen a sus
electrones en los niveles más bajos.
- Un electrón puede abandonar un átomo si recibe suficiente energía, a la cual se le llamará energía de ionización.